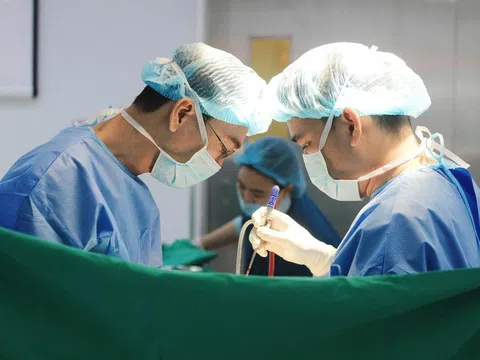
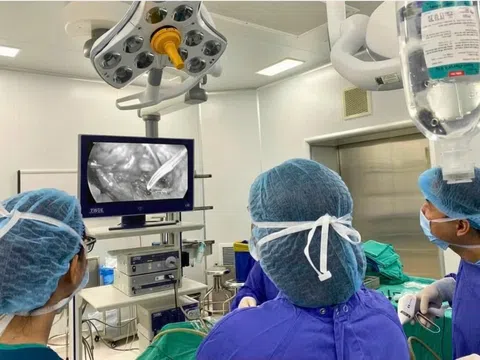
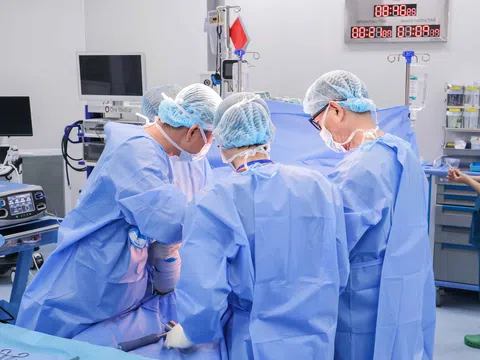
Không ngoa khi nói rằng vaccine COVID-19 đang là vấn đề nóng nhất toàn cầu hiện nay, và cũng khá bất ngờ khi cả ba loại vaccine đang được dùng phổ biến ở Mỹ và trên thế giới là Pfizer, Mordena và Johnson & Johnson đến giờ vẫn chưa được FDA cấp quyền sử dụng đầy đủ, mà chỉ là quyền sử dụng khẩn cấp (emergency use authorization). Và dự kiến đến tháng 9, loại của Pfizer sẽ được phê duyệt đầy đủ.
Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) của Mỹ từ lâu đã nổi tiếng là rất cẩn trọng và nghiêm khắc trong phê duyệt đối với thực phẩm và dược phẩm, và tất cả đều nhằm bảo vệ sức khỏe con người. Và trong tình hình COVID đang hoành hành dữ dội khắp địa cầu hiện nay, FDA nhiều khả năng sẽ cấp quyền sử dụng đầy đủ cho vaccine Pfizer trước lễ Lao động Mỹ 6/9, báo The Hill của Mỹ cho biết ngày 4/8/2021. “Việc xem xét yêu cầu cấp phép của Pfizer được tiến hành càng nhanh càng tốt, phù hợp với các đánh giá hoàn chỉnh và chất lượng cao mà công chúng mong đợi từ FDA”, The Hill trích lời một người phát ngôn của FDA. Tuy nhiên, người phát ngôn này chưa thể thông báo ngày cụ thể để vaccine Pfizer nhận được phê duyệt đầy đủ.
Ngày 7/5, Pfizer nộp hồ sơ xin FDA phê duyệt đầy đủ, và Moderna cũng xin tương tự ngày 1/6. The Hill cho biết Johnson & Johnson sẽ hồ sơ xin FDA cấp phép đầy đủ trong năm 2021 nhưng không rõ lúc nào.
Khi còn đương chức, người tiền nhiệm của Tổng thống Biden là Tổng thống Donald Trump nhiều lần thúc giục FDA nhanh chóng cho phép sử dụng các loại vaccine COVID-19, nhưng FDA không đồng ý mà vẫn theo đúng các quy định nghiêm khắc của mình.
Người hùng của FDA: Cứu sống hàng triệu người
Thập niên 1960, cả thế giới bàng hoàng trước thảm kịch thuốc Thalidomide từ Đức nhưng nước Mỹ đã thoát được nhờ FDA, và kết quả sau đó là sự ra đời của đạo luật của Mỹ về an toàn và quản lý thử nghiệm thuốc.
Năm 1956, thuốc an thần Thalidomide do công ty dược phẩm Grunenthal của Đức sản xuất được tung ra thị trường. Thalidomide được đưa vào danh sách thuốc bán không kê đơn ở Đức và các nước khác vì Grunenthal khẳng định thuốc an toàn với mọi người, kể cả phụ nữ đang mang thai hay nuôi con nhỏ, và trẻ em. Đến năm 1960, Thalidomide đã được tiêu thụ ở rất nhiều nước (không có Mỹ) với doanh số khổng lồ.
Tuy nhiên, giới khoa học và y khoa sau đó phát hiện ra thảm kịch vì thuốc ảnh hưởng nặng đến thai nhi: rất nhiều trẻ được sinh ra với chân và tay bị dị tật nghiêm trọng, gọi là “hội chứng chim cánh cụt” vì tay, chân cực kỳ ngắn với những ngón và đốt không rõ ràng, đôi khi bị dính lại như mái chèo, thậm chí không có tay hoặc chân. Những trẻ em bất hạnh này được kết luận là dị tật do Thalidomide.
Nhưng Thalidomide không có mặt tại nước Mỹ nhờ công của nữ thanh tra FDA tên là Frances Kelsey, người đã cương quyết không cho Thalidomide được phê duyệt ở Mỹ. Tiến sĩ Kelsey cho biết lý do là bà cảm thấy hồ sơ về Thalidomide không cung cấp đầy đủ và toàn diện những dữ liệu về tính an toàn và hiệu quả của thuốc, và bà lo lắng nhất về việc thiếu dữ liệu chứng minh thuốc không ảnh hưởng đến thai nhi. Bà cũng rất lo về việc chưa có bất kỳ kết quả nào từ các thử nghiệm lâm sàng do Mỹ tiến hành đối với loại thuốc này.

Nhờ FDA ngăn chặn thành công Thalidomide, các nhà lập pháp Mỹ thông qua Đạo luật dược phẩm sửa đổi Kefauver-Harris năm 1962 để bắt buộc tất cả các loại thuốc phải trải qua thử nghiệm tiền lâm sàng để chứng minh tính an toàn và hiệu quả. Tháng 8/1962, Tổng Thống John Kennedy trao cho Tiến sĩ Kesley Huân Chương của Tổng thống dành cho người cống hiến xuất sắc cho dịch vụ dân sinh.
Câu chuyện về thảm kịch Thalidomide và thái độ nghiêm khắc và cương quyết của FDA Mỹ là một bài học để đời cho lĩnh vực dược và y khoa toàn thế giới.